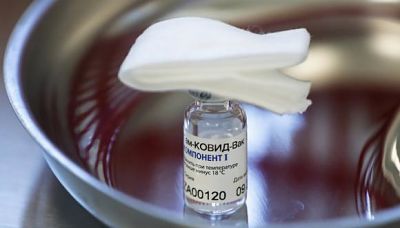
Brasil rechazó la solicitud para evaluar el uso de emergencia de la vacuna rusa Sputnik V
La Agencia Nacional de Vigilancia Sanitaria de Brasil (Anvisa) rechazó la solicitud de autorización de emergencia de la vacuna rusa Sputnik V, según un comunicado publicado por el organismo.
Según detalla el texto, la razón es que los documentos no presentaban “requisitos mínimos de presentación y análisis, y las cuestiones relacionadas con las buenas prácticas de fabricación”. La solicitud -finalmente vetada- para el uso de emergencia de 10 millones de dosis de la vacuna rusa fue presentada por la compañía farmacéutica União Química el viernes 15 de enero.
En el comunicado, Anvisa citó la falta de estudios clínicos sobre la vacuna de fase tres. La semana pasada, la agencia determinó como uno de los criterios para la solicitud y el uso de emergencia de la vacuna que el laboratorio lleve a cabo la fase tres de los estudios - la fase de análisis clínico - en Brasil.
Hasta ahora, el desarrollo ruso no ha iniciado esta etapa del proceso en territorio brasileño. El organismo aclara que no basta con que la solicitud de autorización de la fase tres del ensayo clínico se presente para uso de emergencia. Es necesario que esos estudios estén en curso en el país.
Según el organismo, la solicitud de autorización de uso de emergencia “debe incluir estrategias que el solicitante aplicará para garantizar que los ensayos clínicos en curso de la vacuna puedan evaluar la seguridad y la eficacia a largo plazo”.
...
100 días de Biden, un profundo cambio en el rumbo de EEUU en El Día
Brasil anuncia vacuna propia en El Día
España también paraliza la vacunación con AstraZeneca en El Día
AstraZeneca pidió en Brasil el registro definitivo de su vacuna contra el coronavirus en El Día
Una dosis de vacuna podría ser efectiva contra Covid-19 en El Diario
La vacuna china es la única lista en Brasil para empezar la inmunización en Los Tiempos
Brasil decide el domingo sobre el uso de vacunas con carácter de emergencia en Los Tiempos
